12 — 14 марта в Лугано прошла ежегодная конференция ESMO Sarcoma and Rare Cancers, и на сессии коротких устных докладов были представлены новые данные по лечению и биологии редких опухолей и сарком. Представляем наиболее интересные из них и применимые в реальной практике.
Автор: Тарарыкова Анастасия Алексеевна
Врач-онколог отдела общей онкологии НИИ клинической онкологии им. акад. РАН и РАМН Н.Н. Трапезникова ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России, эксперт Восточно-европейской саркомной группы и Ассоциации специалистов по изучению сарком, кандидат медицинских наук, Москва
Одним из наиболее заметных результатов стала высокая активность комбинации озекибарта (DR5-агонист) с иринотеканом + темозоламидом (I/T) у пациентов с рецидивной или рефрактерной саркомой Юинга (84МО) [1]. Саркома Юинга остается одной из наиболее агрессивных опухолей костей и мягких тканей у детей, подростков и молодых взрослых, а результаты лечения при рецидиве остаются неудовлетворительными. Например, в исследовании rEECur объективный ответ на режим I/T по 5-дневной схеме составлял около 20%. Ранее комбинация озекибарт с I/T уже продемонстрировала предварительную противоопухолевую активность (ORR 71,4%) в ранних этапах этого же исследования.
В представленную расширенную когорту открытого исследования I фазы были включены пациенты с местнораспространенной или метастатической нерезектабельной классической саркомой Юинга (EWSR1::ETS fusion). К участию допускались пациенты в возрасте ≥12 и <85 лет, получившие 1-2 линии предшествующей системной терапии, при этом предшествующее лечение иринотеканом и/или темозоломидом допускалось. Озекибарт вводился в дозе 3 мг/кг в 1-й день, а иринотекан и темозоломид назначались в 1-5-й дни 21-дневного цикла. После ≥6 циклов химиотерапия могла быть отменена по решению исследователя в связи с потенциальной токсичностью, тогда как терапия озекибартом продолжалась. Основными конечными точками исследования были безопасность и клинический ответ.
По состоянию на дату отсечки данных 15 октября 2025 года лечение комбинацией озекибарт + I/T получили 32 пациента. Медиана возраста составила 31 год (диапазон 13-71 год), а медиана числа предшествующих линий терапии – 2. Ранее иринотекан и/или темозоломид получали 4 пациента. На момент анализа 13 пациентов продолжали лечение, 4 пациента прекратили терапию из-за нежелательных явлений (при этом ни одно из них не было связано с озекибартом, а 2 случая были связаны с режимом I/T) и у 14 пациентов было зарегистрировано прогрессирование заболевания.
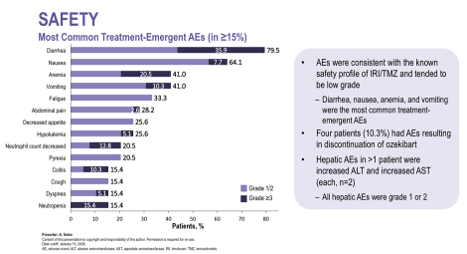
Профиль безопасности в целом соответствовал известной токсичности комбинации иринотекан/темозоломид. Наиболее частыми нежелательными явлениями были диарея (78,1% всех степеней; ≥3 степени – 34,4%), тошнота (68,8%; ≥3 степени – 9,4%), анемия (46,9%; ≥3 степени – 28,1%) и рвота (43,8%; ≥3 степени – 9,4%). Случаев гепатотоксичности ≥3 степени не наблюдалось.
На момент анализа 25 пациентов были оценимы по эффективности терапии. Объективный ответ (ORR) при применении комбинации озекибарт + I/T составил 68,0% (17/25), при этом все ответы были частичными. Примечательно, что один из пациентов, достигших ответа, ранее уже прогрессировал на режиме, содержащем иринотекан. Контроль заболевания был достигнут у 92,0% пациентов (23/25). У одного пациента заболевание оставалось без признаков прогрессирования примерно через 22 месяца терапии.
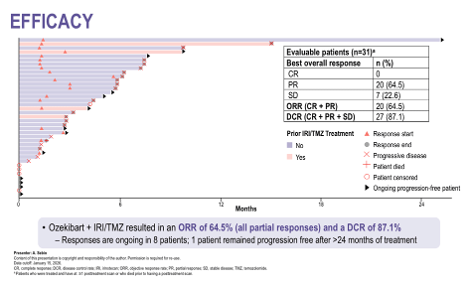
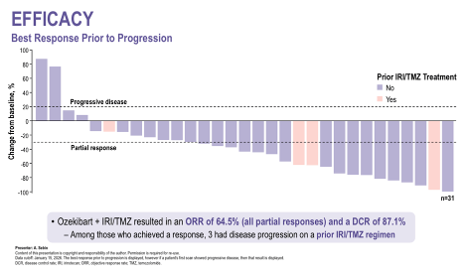
Рисунки 2, 3. Эффективность терапии.
Таким образом, комбинация озекибарта с иринотеканом и темозоломидом продемонстрировала высокую частоту объективных ответов (68,0%) и управляемый профиль безопасности у пациентов с рецидивирующей или рефрактерной саркомой Юинга. Полученные результаты поддерживают дальнейшее клиническое изучение данного подхода в этой популяции пациентов.
Представлены результаты объединенного анализа двух проспективных исследований II фазы – DOREMY (лучевая терапия 36 Гр/18 фракций) и LIPOMYX (25 Гр/5 фракций), посвященных оценке эффективности сниженных доз предоперационной лучевой терапии у пациентов с первичной миксоидной липосаркомой (MLPS), подтипом саркомы мягких тканей, известным своей высокой радиочувствительностью (82МО) [2].
В анализ были включены 87 пациентов, которым проводилась предоперационная лучевая терапия по одной из двух схем (36 или 25 Гр), после чего выполнялась органосохраняющая операция. При морфологическом исследовании резецированных опухолей оценивались такие параметры патологического ответа, как гиалиноз, жировая дифференцировка и некроз. Клинические конечные точки включали частоту R0-резекций, локальный контроль, безметастатическую выживаемость (DMFS) и общую выживаемость (OS).
Высокое качество хирургического лечения было достигнуто у большинства пациентов: R0-резекция выполнена в 94,3% случаев, при этом локальный контроль составил 100%. В течение наблюдения 9 пациентов (10%) развили отдаленные метастазы. Долгосрочные результаты лечения также оказались благоприятными: 4-летняя безметастатическая выживаемость (DMFS) составила 82,8%, а 4-летняя общая выживаемость (OS) – 90,1%. Статистически значимых различий между режимами 36 и 25 Гр по показателям DMFS выявлено не было (p=0,27). Частота раневых осложнений также не различалась между группами (p=0,5).
Гистологический анализ показал, что терапевтический эффект в большей степени характеризовался стромальными изменениями, а не выраженным опухолевым некрозом. Средняя доля гиалиноза составила 48%, жировой дифференцировки – 25%, некроза – 9,5%, тогда как доля жизнеспособной опухолевой ткани составляла в среднем 17%. Комбинация гиалиноза и жировой дифференцировки наблюдалась у 73% пациентов.
При сравнении режимов отмечены некоторые различия в морфологическом ответе. Схема 36 Гр ассоциировалась с более выраженной гиалинизацией (медиана 50% против 25%, p=0,003) и большей долей комбинированных стромальных изменений. В то же время режим 25 Гр сопровождался более высокой долей некроза (5% против 0%, p=0,04). Однако параметры патологического ответа в целом не коррелировали с безметастатической выживаемостью, за исключением пограничной тенденции к худшему прогнозу при более выраженном некрозе (p=0,0502).
Таким образом, оба режима сниженной дозы предоперационной лучевой терапии демонстрируют эффективность у пациентов с миксоидной липосаркомой, обеспечивая хорошие показатели локального контроля и высокую частоту радикальных резекций. Полученные данные также подтверждают, что морфологический ответ при MLPS преимущественно представлен стромальными изменениями, а не некрозом (а мы видели это и ранее). Результаты исследования поддерживают возможность использования коротких предоперационных схем радиотерапии с меньшей суммарной дозой у данного радиочувствительного подтипа сарком.
Представлены результаты ретроспективного исследования, посвященного клинико-патоморфологическим характеристикам и прогнозу пациентов с первичными саркомами головного мозга – крайне редкой группе мезенхимальных опухолей центральной нервной системы, составляющих небольшую долю внутричерепных злокачественных новообразований (80МО) [3]. Анализ был выполнен на основе данных регистра SEER и включал пациентов, у которых диагноз первичной саркомы головного мозга был установлен в период 2000-2022 годов.
В итоговый анализ были включены 266 пациентов. Большинство больных были относительно молодыми: 71,1% пациентов были моложе 60 лет. Наиболее частыми локализациями опухолей оказались лобная доля (29,6%), теменная доля (15,7%) и височная доля (15,3%). Среди гистологических вариантов преобладали солитарная фиброзная опухоль (32,7%), NOS саркома (20,3%), веретеноклеточная саркома (9%) и рабдомиосаркома (7,1%). На момент постановки диагноза заболевание чаще всего выявлялось на ранних стадиях: локализованная стадия отмечена у 74,4% пациентов, а локально-распространенная – у 17,9%.
Основным методом лечения оставалось хирургическое вмешательство, которое было выполнено у 87,9% пациентов. Лучевая терапия применялась у 58,2%, а химиотерапия – у 25,9% пациентов. Метастатическое поражение наблюдалось относительно редко: наиболее частыми локализациями метастазов были легкие (2,6%) и печень (1,1%).
Анализ выживаемости показал относительно благоприятные показатели для данной редкой патологии. 1-летняя выживаемость составила 75%, 3-летняя – 63,4%, а 5-летняя – 57,7%. Медиана общей выживаемости достигала 106 месяцев (95% ДИ 35,6-176,3). В ходе многовариантного анализа были определены независимые прогностические факторы, влияющие на исход заболевания, включая возраст пациента, пол, гистологический тип саркомы, стадию заболевания на момент диагностики, а также проведение лучевой терапии.

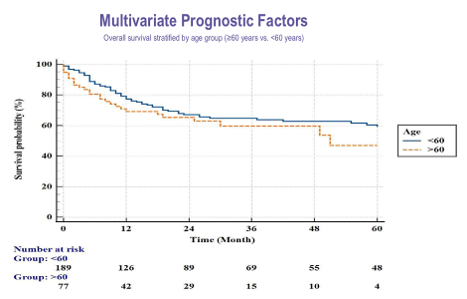
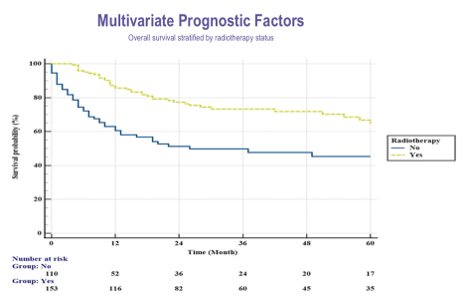
Рисунки 4-6. Прогностические факторы и показатели ОВ в зависимости от возраста и проведения ЛТ.
Таким образом, результаты исследования показывают, что ключевыми факторами, определяющими прогноз у пациентов с первичными саркомами головного мозга, являются стадия заболевания и гистологический подтип опухоли. Несмотря на то, что хирургическое лечение остается основным терапевтическим подходом, лучевая терапия также демонстрирует независимое влияние на выживаемость, что подчеркивает ее значимую роль в комплексном лечении этой редкой группы опухолей.
И последнее исследование, которое хочется осветить, – результаты крупного сравнительного анализа эффективности пембролизумаба во второй линии лечения пациентов с распространенными саркомами мягких тканей после химиотерапии на основе адриамицина (83МО) [4]. Несмотря на ранее продемонстрированную противоопухолевую активность ингибиторов PD-1 при отдельных подтипах сарком, прямые сравнительные данные реальной клинической практики с другими вариантами второй линии терапии до настоящего времени оставались ограниченными.
Исследование было выполнено на основе базы TriNetX Global Collaborative Network, объединяющей анонимизированные клинические данные из медицинских учреждений по всему миру. В анализ были включены пациенты, получавшие один из пяти вариантов системной терапии во второй линии: пембролизумаб (Pe), трабектедин (T), эрибулин (E), комбинацию гемцитабин + доцетаксел (GD) или пазопаниб (Pa). Основной конечной точкой исследования была 5-летняя общая выживаемость. Для анализа выживаемости применялись методы Kaplan-Meier, рассчитывались отношения рисков (HR) и 95% доверительные интервалы, а для минимизации возможных различий между группами использовался метод propensity score matching (PSM) с балансировкой по возрасту, полу и расе.
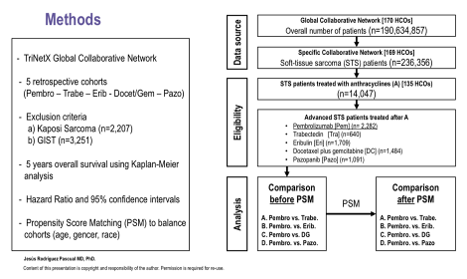
Рисунок 7.
Всего в исследование были включены 7197 пациентов, распределенных следующим образом: 2282 пациента получали пембролизумаб, 1484 – гемцитабин + доцетаксел, 631 – трабектедин, 1709 – эрибулин и 1091 – пазопаниб. После применения метода PSM терапия пембролизумабом продемонстрировала статистически значимое преимущество по общей выживаемости по сравнению со всеми другими режимами второй линии. Так, при сравнении с трабектедином отношение рисков составило HR 0,615 (p<0,0001), с эрибулином – HR 0,316 (p<0,0001), с комбинацией гемцитабин + доцетаксел – HR 0,529 (p<0,0001), а с пазопанибом – HR 0,510 (p<0,0001).
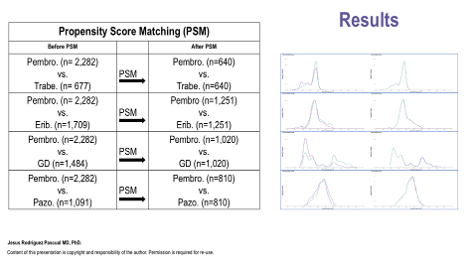
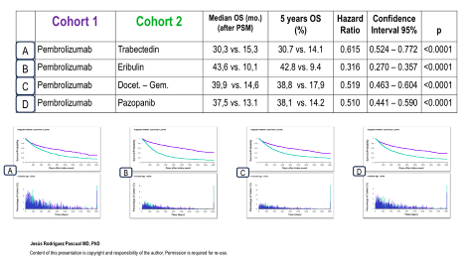
Рисунки 8-9. Результаты в когортах.
Полученные данные свидетельствуют о том, что в условиях реальной клинической практики применение пембролизумаба после антрациклин-содержащей химиотерапии может ассоциироваться с более благоприятными показателями общей выживаемости по сравнению с рядом стандартных режимов второй линии, включая трабектедин, эрибулин, комбинацию гемцитабин + доцетаксел и пазопаниб, у пациентов с распространенными саркомами мягких тканей.
Источники:
- Ana Sebio Garcia (Barcelona, Spain), et al. 84MO – Phase I study of the tetravalent death receptor 5 (DR5) agonist ozekibart (INBRX-109) combined with irinotecan (I) and temozolomide (T) in adolescents and adults with Ewing sarcoma.
- Hanna M. Kosela Paterczyk (Warsaw, Poland), et al. 82MO – Pooled analysis of two prospective trials on reduced dose preoperative radiotherapy in primary myxoid liposarcoma – correlation of pathologic responses and treatment outcomes.
- Halis Yerlikaya (Ankara, Türkiye), et al. 80MO – Evaluation of clinicopathological features and prognoses of patients with brain sarcoma.
- Jesus Rodriguez Pascual (Madrid, Spain), et al. 83MO – Pembrolizumab after adriamycin-based chemotherapy in patients with soft-tissue sarcoma: A real-world comparative analysis of second-line efficacy.

